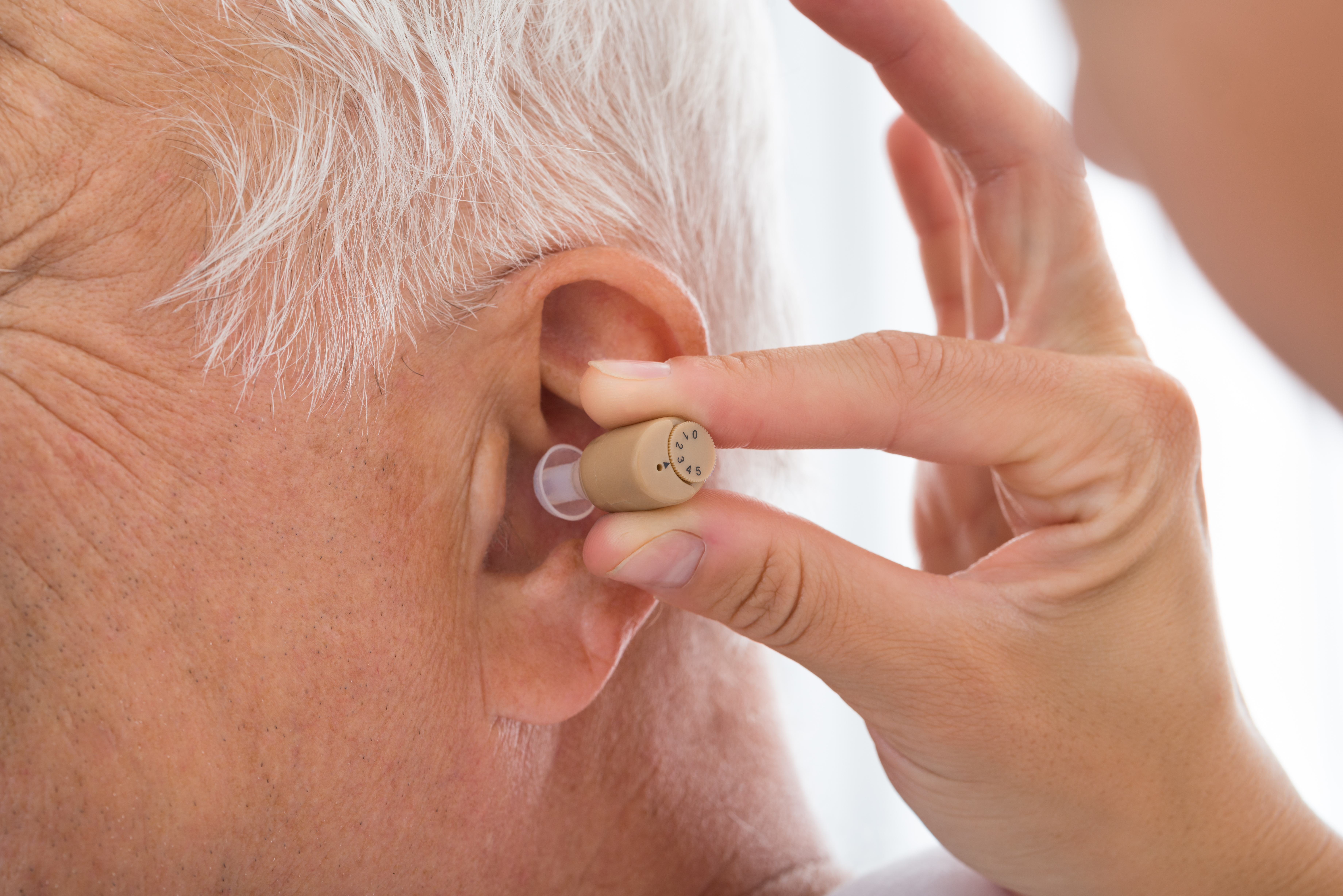
基因组学与个性化用药的最新突破
基因组学与个性化用药正结合多学科技术,推进从群体疗法向个体化治疗的转变。近年来,测序成本下降、AI 辅助解读能力提升、可穿戴设备的数据流入,以及数据互操作性改进,共同推动临床决策更精准。本文概述关键技术进展、临床应用场景、数据安全挑战以及未来发展方向,帮助读者理解基因信息如何改变用药选择与慢性病管理。

随着基因组学研究与临床应用的加速,个性化用药(precision medicine)正在逐步从理论走向实践。高通量测序、群体数据库和功能基因组学让药物反应的遗传基础更加清晰;同时,人工智能(AI)和预测分析(predictiveanalytics)能够从海量基因与临床数据中提取可操作洞见。可穿戴设备与数字疗法(digitaltherapeutics)提供连续的表型数据,支持对慢性病(chroniccare)患者的长期管理。尽管前景广阔,数据互操作性(interoperability)、隐私与数据安全(privacy、datasecurity)问题仍需优先解决,以确保临床部署的可靠性与合规性。
本文仅供信息参考,不应视为医疗建议。请咨询合格的医疗专业人员以获取个性化的指导和治疗。
基因组学的最新技术突破 (genomics)
近年来,测序成本持续下降且准确性提升,新一代测序(NGS)和长读长测序技术使罕见变体和结构变异的检测更为可靠。功能注释和多组学数据融合(如转录组、蛋白质组)帮助将基因变异与药物代谢途径直接关联,为药代动力学和药效学的预测提供依据。此外,群体遗传学数据库的扩展改善了不同人群用药反应的参考背景,降低了误判风险。
个性化用药如何体现 precisionmedicine?
个性化用药不只是根据基因型调整剂量,还包括选择更合适的药物类别、识别潜在不良反应风险以及制定随访策略。药物基因组学(pharmacogenomics)能在临床处方前预判代谢酶活性差异(例如 CYP450 相关变异),从而避免无效治疗或严重副作用。在临床路径中引入基因组结果的标准化解读和临床决策支持,有助于将 precisionmedicine 从试点推广到常规医疗实践。
AI 在用药决策中的作用 (ai)
AI 与机器学习模型可整合基因组、影像、电子病历和可穿戴设备输出,提供个体化风险评估与疗效预测。解释性模型和因果推断技术正在改进模型透明度,以便医生理解模型推荐背后的生物学依据。值得注意的是,训练数据的多样性直接影响模型泛化能力,因此在开发 AI 系统时必须纳入不同人群的基因和临床数据,避免系统性偏差。
预测分析与数据保护 (predictiveanalytics / datasecurity / privacy)
预测分析可以识别高风险用药组合与潜在不良反应,但依赖于敏感基因数据与长期健康记录。这带来隐私与数据安全挑战,包括基因隐私、数据滥用风险和再识别问题。合规的数据治理、加密存储、多方安全计算和差分隐私等技术,是在保护个人隐私的同时实现模型训练与临床应用的关键。政策层面也需明确基因数据的使用边界与患者同意机制。
可穿戴设备与数字疗法在慢性病管理中的结合 (wearables / digitaltherapeutics / chroniccare)
可穿戴设备提供心率、活动量、睡眠和葡萄糖等连续表型数据,补充基因组学的静态信息。数字疗法可以基于这些实时信号与基因风险实现动态调整的治疗方案,例如调整药物剂量或提示行为干预,从而改善慢性病患者的长期结局。实现这一闭环需要设备与电子病历的互操作性以及对数据质量和可靠性的严格验证。
互操作性与价值型医疗 (interoperability / valuebasedcare / mentalhealth)
将基因组信息纳入临床工作流要求不同系统间的高效互操作(interoperability),包括标准化的报告格式、API 接口与临床决策支持工具。只有在互操作的环境中,基因组学的价值才能体现在价值型医疗(valuebasedcare)指标上,例如降低不良事件率或提高治疗有效率。心理健康(mentalhealth)领域也在探索基因与生活方式数据相结合的个体化干预,但需要谨慎解读遗传风险对行为与治疗反应的影响。
结论:基因组学与个性化用药的结合正在通过技术整合改变临床实践,从精准的药物选择到个体化慢性病管理均显现出潜力。未来的关键在于提升数据互操作性、确保算法公平与透明、并建立健全的隐私与安全框架,以便在保护患者权益的同时,真正实现基于证据的个性化治疗。